(Last Paragraph)
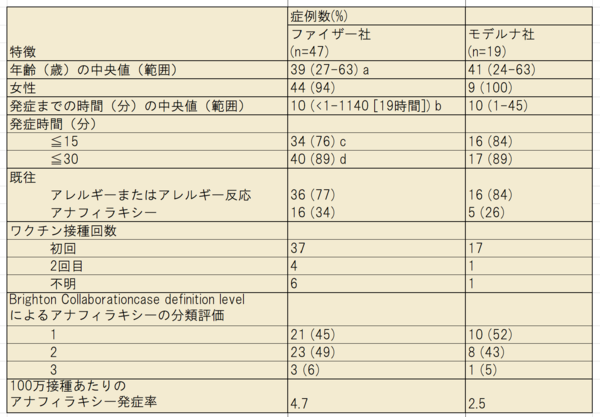
Continued safety monitoring of mRNA COVID-19 vaccines in the US has confirmed that anaphylaxis following vaccination is a rare event, with rates of 4.7 cases/million Pfizer-BioNTech vaccine doses administered and 2.5 cases/million Moderna vaccine doses administered, based on information through January 18, 2021. When considered in the context of morbidity and mortality from COVID-19, the benefits of vaccination far outweigh the risk of anaphylaxis, which is treatable. Because of the acute, life-threatening nature of anaphylaxis, immediate epinephrine administration is indicated for all cases. CDC guidance on use of mRNA COVID-19 vaccines and management of anaphylaxis is available. All facilities administering COVID-19 vaccines should have the necessary supplies and trained medical personnel available to manage anaphylaxis.
(最終段落)
米国におけるmRNA COVID-19ワクチンの安全性モニタリングを継続して行った結果、2021年1月18日までの情報によると、ファイザー・バイオンテック社のワクチン投与では4.7例/百万本、モデルナ社のワクチン投与では2.5例/百万本と、ワクチン接種後のアナフィラキシーの発生は稀であることが確認された。COVID-19による罹患率と死亡率を考慮すると、ワクチン接種の利点は、治療可能なアナフィラキシーのリスクをはるかに上回っている。アナフィラキシーのもつ急性で生命を脅かす性質のため、すべての症例でエピネフリンの即時投与が必要である。mRNA COVID-19 ワクチンの使用およびアナフィラキシーの管理に関する CDC のガイダンスがある。COVID-19ワクチンを投与するすべての施設は、アナフィラキシーを管理するために必要な物資と訓練を受けた医療従事者を用意しなければならない.
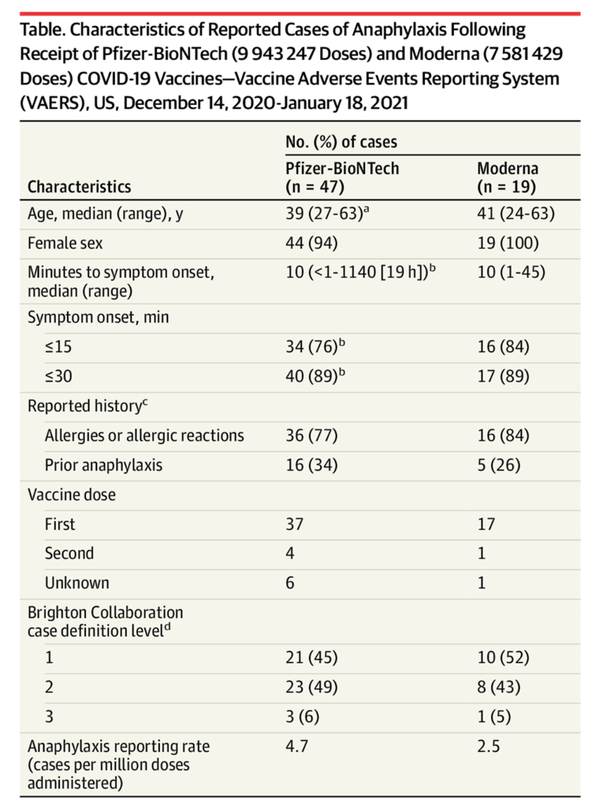
<表>ファイザー・バイオンテック(9,943,247 投与)およびモデナ(7,581,429 投与)の接種後に報告されたアナフィラキシーの特徴 COVID-19 ワクチン-ワクチン有害事象報告システム(VAERS)、米国、2020年12月14日~2021年1月18日
注
a Pfizer-BioNTech社の報告書1件で年齢が欠落している。
b BioNTech社の報告書2件で症状発現までの時間が欠落している。
c 狂犬病ワクチン、インフルエンザA(H1N1)ワクチン、季節性インフルエンザワクチン、不特定のワクチン、ガドリニウム・ヨウ素系造影剤、不特定の静脈内造影剤、不特定の輸液、サルファ剤、ペニシリン、プロクロルペラジン、ラテックス、クルミ、不特定の木の実、クラゲ刺傷、不特定の複数の環境・食物アレルゲン、不特定の曝露。
d ブライトンコラボレーションの症例定義では、症状の組み合わせを用いて診断の確実性のレベルを定義している。ブライトンレベル1は、報告された症例がアナフィラキシーを表すという診断上の確実性の最高レベルを表し、レベル2と3は診断上の確実性の低いレベルを表している。レベル4はアナフィラキシーとして報告されたが、ブライトンコラボレーションの症例定義を満たしていない症例であり、レベル5はアナフィラキシーとして報告されていない上に症例定義を満たしていない症例である。
https://jamanetwork.com/journals/jama/fullarticle/2776557