Vaccines are needed to prevent coronavirus disease 2019 (Covid-19) and to protect persons who are at high risk for complications. The mRNA-1273 vaccine is a lipid nanoparticle-encapsulated mRNA-based vaccine that encodes the prefusion stabilized full-length spike protein of the severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2), the virus that causes Covid-19.
This phase 3 randomized, observer-blinded, placebo-controlled trial was conducted at 99 centers across the United States. Persons at high risk for SARS-CoV-2 infection or its complications were randomly assigned in a 1:1 ratio to receive two intramuscular injections of mRNA-1273 (100 μg) or placebo 28 days apart. The primary end point was prevention of Covid-19 illness with onset at least 14 days after the second injection in participants who had not previously been infected with SARS-CoV-2.
The trial enrolled 30,420 volunteers who were randomly assigned in a 1:1 ratio to receive either vaccine or placebo (15,210 participants in each group). More than 96% of participants received both injections, and 2.2% had evidence (serologic, virologic, or both) of SARS-CoV-2 infection at baseline. Symptomatic Covid-19 illness was confirmed in 185 participants in the placebo group (56.5 per 1000 person-years; 95% confidence interval [CI], 48.7 to 65.3) and in 11 participants in the mRNA-1273 group (3.3 per 1000 person-years; 95% CI, 1.7 to 6.0); vaccine efficacy was 94.1% (95% CI, 89.3 to 96.8%; P<0.001). Efficacy was similar across key secondary analyses, including assessment 14 days after the first dose, analyses that included participants who had evidence of SARS-CoV-2 infection at baseline, and analyses in participants 65 years of age or older. Severe Covid-19 occurred in 30 participants, with one fatality; all 30 were in the placebo group. Moderate, transient reactogenicity after vaccination occurred more frequently in the mRNA-1273 group. Serious adverse events were rare, and the incidence was similar in the two groups.
The mRNA-1273 vaccine showed 94.1% efficacy at preventing Covid-19 illness, including severe disease. Aside from transient local and systemic reactions, no safety concerns were identified.
COVID-19を予防し、合併症のリスクが高い人を守るためにはワクチンが必要である。mRNA-1273ワクチンは、COVID-19の原因ウイルスである重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)の前駆安定化全長スパイクタンパク質をコードする脂質ナノ粒子カプセル化mRNAベースのワクチンである。
この第 3 相無作為化観察者盲検プラセボ対照試験は、米国内の 99 施設で実施された。SARS-CoV-2感染またはその合併症のリスクが高い人を1:1の割合で無作為に割り付け、mRNA-1273(100μg)を28日間隔で2回筋肉内注射する群とプラセボを28日間隔で投与する群に分けた。主要エンドポイントは、SARS-CoV-2に感染したことのない参加者において、2回目の注射から少なくとも14日後時点でのCOVID-19の予防であった。
この試験では、30,420人のボランティアが登録され、1対1の割合でワクチンまたはプラセボのいずれかの投与を受けるように無作為に割り付けられた(各群15,210人)。96%以上の参加者が両方の注射を受け、ベースライン時にSARS-CoV-2感染の証拠(血清学的、ウイルス学的、またはその両方)を持っていたのは2.2%であった。プラセボ群185人(1000人年あたり56.5人;95%信頼区間[CI]、48.7~65.3)およびmRNA-1273群11人(1000人年あたり3.3人;95%CI、1.7~6.0)で症状のあるCOVID-19感染が確認され、ワクチンの有効性は94.1%(95%CI、89.3~96.8%;P<0.001)であった。有効性は、初回接種から 14 日後の評価、ベースライン時に SARS-CoV-2 感染の証拠を有する参加者を含む解析、65 歳以上の参加者を対象とした解析を含む主要な副次的解析でも同様であった。重度のCOVID-19は30人の参加者に発生し、1人が死亡した;30人全員がプラセボ群であった。ワクチン接種後の中等度の一過性の反応原性は、mRNA-1273群でより頻繁に発生した。重篤な有害事象はまれであり、発生率は両群で同程度であった。
mRNA-1273 ワクチンは、重症化を含むCOVID-19 の予防に 94.1%の有効性を示した。一過性の局所反応および全身反応を除いて、安全性に関する懸念は認められなかった。
Figure3
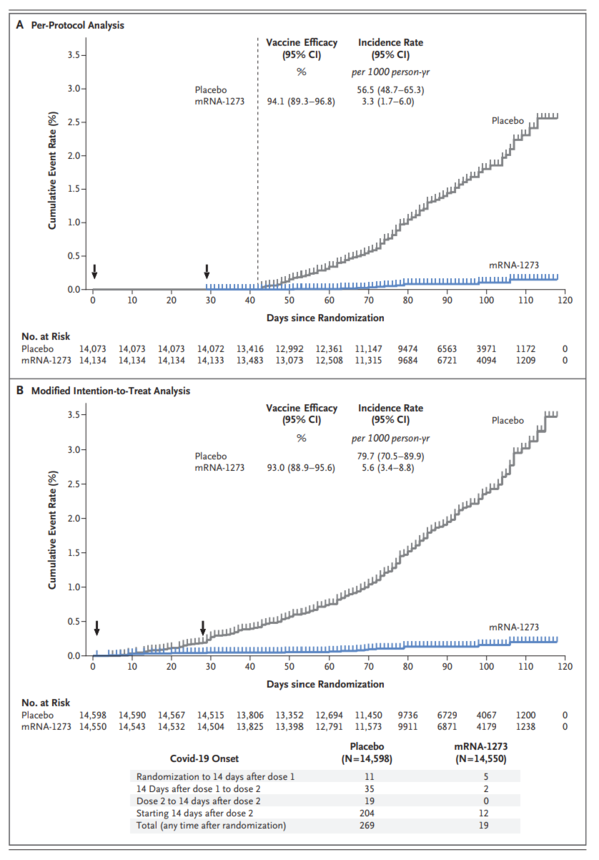

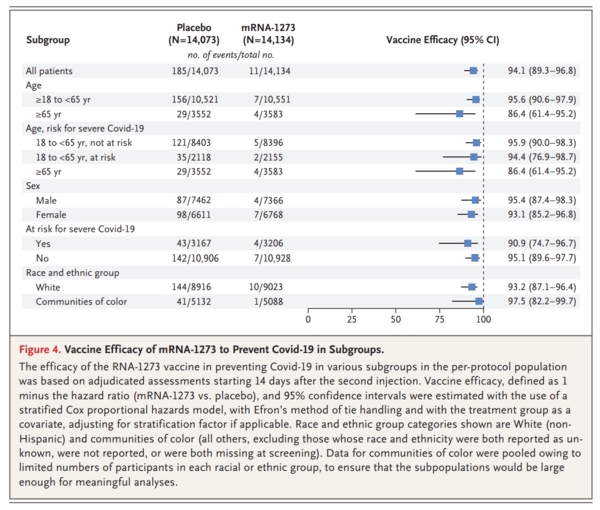
Figure4
https://www.nejm.org/doi/pdf/10.1056/NEJMoa2035389?articleTools=true